Neurobiologia del envejecimiento parte 1
Neurobiología del envejecimiento
El envejecimiento es un proceso biológico
unidireccional que se caracteriza, principalmente, por una disminución de las
funciones que hacen más susceptible al ser humano de padecer enfermedades y
morir a consecuencia de ellas (Nilsen, 2008).
En este proceso el organismo va perdiendo la habilidad para responder ante
el estrés y mantener la regulación homeostática y metabólica; teniendo como
consecuencia la disminución de las capacidades cognitivas y de sobrevivencia
(Glica et al., 2009).
A través de los años, el individuo comienza a envejecer y esto hace que
aparezcan cambios irreversibles que afectan células, tejidos y órganos o la
totalidad del individuo. Por lo tanto la vejez no es una enfermedad, aun cuando
en cierto número de ancianos se desarrollan discapacidades por la falta de una
respuesta adecuada a los agentes estresantes del medio ambiente (Zorrilla,
2002).
Alteraciones funcionales por
la edad
Conforme avanza la edad, ocurren alteraciones en las funciones mentales, la coordinación motora y los patrones del sueño; disminuyen el peso y volumen cerebral, debido a la reducción de neuronas y vasos sanguíneos, y aumentan las neuronas atróficas. La sustancia gris se reduce a partir de la 3a. década de la vida y la sustancia blanca entre la 6a y la 7a décadas. A lo largo de la vida el cerebro sufre una serie de modificaciones estructurales, microscópicas, macroscópicas y bioquímicas.
Estas alteraciones se relacionan con cambios
neuroendocrinos, ante los que este sistema es altamente sensible al
envejecimiento, el cual provoca un decremento abrupto y gradual en la
circulación hormonal.
Envejecimiento: teorías del
porqué envejecemos y defensa natural contra el envejecimiento
Existen diversas teorías del por qué ocurre el envejecimiento. Una de éstas
es que las células normales están programadas para un número determinado de
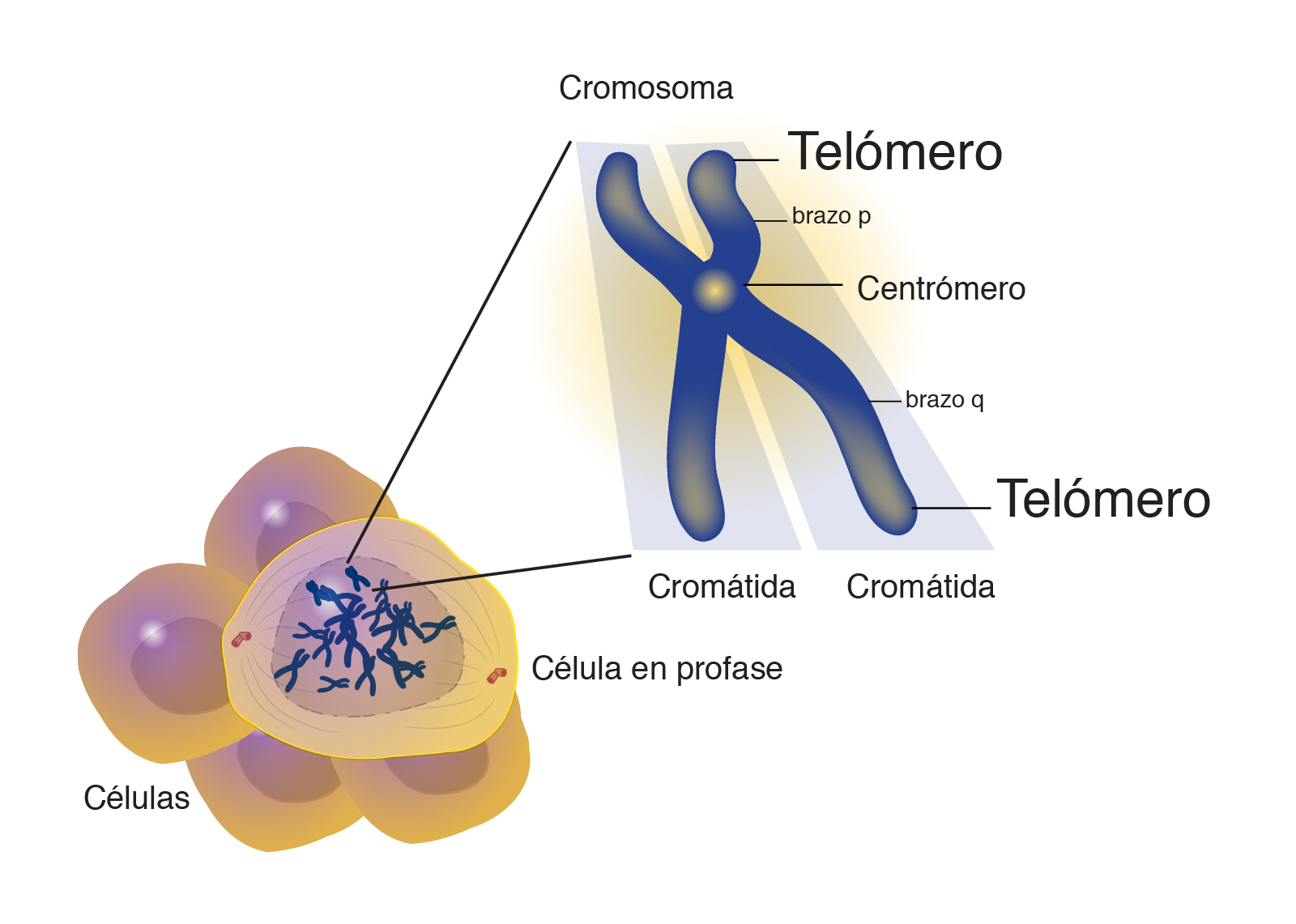
divisiones. Cada cromosoma posee en sus extremos una serie de secuencias
altamente repetitivas y no codificantes, denominadas telómeros éstos se van acortando con las divisiones
sucesivas.
Por envejecimiento, este acortamiento progresivo de los telómeros
cromosómicos desencadena la muerte celular, representando una especie de reloj
genético que determinaría el tiempo de vida de las células.
Otra teoría se refiere a la regulación por genes del envejecimiento, los
cuales juegan un papel importante en la expresión de proteínas (Howitz et al.,
2003; Sauve et al., 2006) siendo la teoría proteómica y otra mas se refiere al
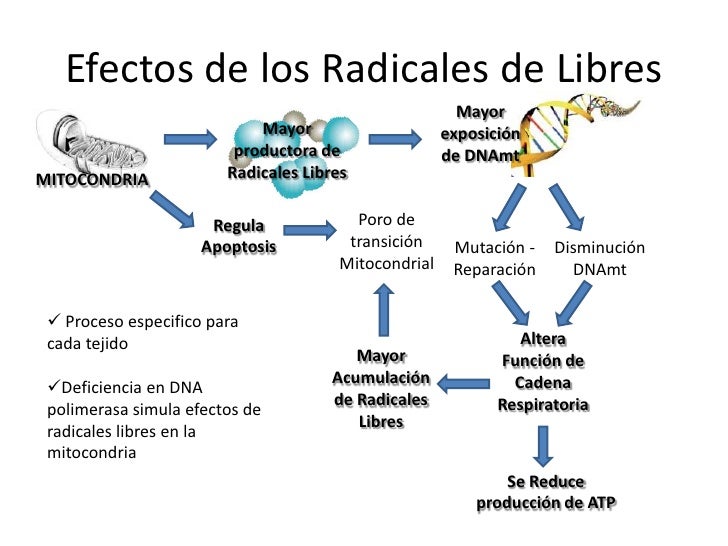
estrés oxidativo, en donde hay una disfunción de las mitocondrias incrementada por el daño oxidativo a sus membranas,
en donde los agentes oxidantes se acumulan con la edad dentro de las células
alterando las diversas funciones internas de las mitocondrias, siendo
irreversible por lo que se asocia con el envejecimiento por el aumento el daño
celular, de tejidos y de todo el organismo (Shigenaga et al., 1994).
¿Porque unas personas
envejecen mas que otras?
Las causas normales del envejecimiento tienen que ver con el tipo de vida
de las personas, pero indudablemente se acelera por los factores de riesgo
medioambientales, como la contaminación o el consumo de enervantes y todos los
factores que propician el incremento de elementos capaces de oxidar las células
conocidas como prooxidantes, entre ellos los radicales libres.
Se sabe que el metabolismo crea subproductos (en particular, los radicales
libres) capaces de dañar las células, por lo que la velocidad del metabolismo
de un individuo (tipo de vida) condiciona su envejecimiento.
Cada célula, de la especie animal que sea, tendría así el mismo capital
metabólico, o consumo energético. Las células, y en consecuencia el organismo,
envejecerían así según el consumo de este capital.
Teoría de los radicales
libres
Esta teoría postula que el daño sostenido, infligido por la exposición
ininterrumpida por oxidantes, es el punto fundamental detrás de la pérdida de
la función celular y de su vitalidad (Shigenaga et al., 1994).
El organismo contrapone la acción de antioxidantes para desintoxicar
rápidamente los reactivos intermedios o reparar el daño de las estructuras
biológicas resultantes (Sies, 1991).
Pero cuando el equilibrio entre radicales libres y antioxidantes se pierde
en favor de los primeros, se genera el estrés oxidativo, desencadenando una serie
de procesos dañinos que se asocian al desarrollo de numerosas enfermedades (ateroesclerosis, cáncer, cataratas,
depósitos de minerales como el hierro y cobre en diferentes áreas del cerebro,
diabetes, artritis, inflamaciones crónicas y neuropatologías como la enfermedad
de Parkinson y Alzheimer).
Asimismo, el proceso biológico
del envejecimiento se acelera en relación directa con la magnitud del estrés
oxidativo y su relación con
alteraciones metabólicas y deficiencia cognitiva. Un aspecto relevante, aunado al aspecto clínico, es el manejo
inadecuado en los criterios diagnósticos entre envejecimiento normal y patológico (Butterfield and
Lauderback, 2002).
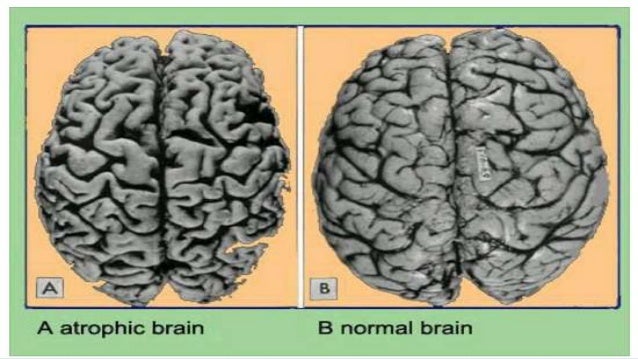
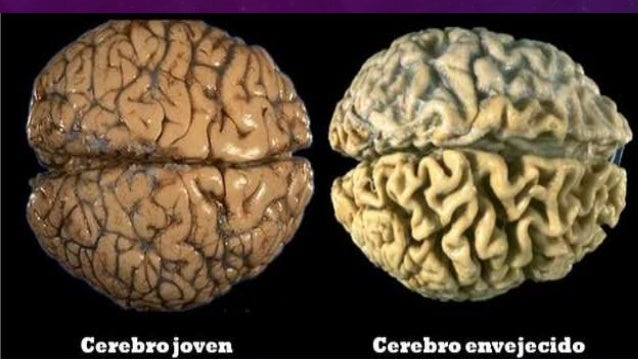
El envejecimiento cerebral
No puede ser considerado sólo desde un punto de vista cronológico sino
también a través de una perspectiva morfológica y funcional. La “edad
cronológica” consigna que el proceso de envejecer comienza entre los 60 y 65
años, aunque para las neuronas empieza alrededor de los 30 años, por lo que
diferentes sistemas del organismo no envejecen a la misma velocidad. Es
probable que un cerebro viejo sea consecuencia del deterioro de otros sistemas
como el cardiovascular o endocrino, aunado al propio proceso de envejecimiento
cerebral.
·
Envejecimiento
en la mujer
Durante el proceso de envejecimiento en la mujer, se advierte la pérdida de los esteroides sexuales lo que en parte, puede explicar el deterioro cognitivo y la neurodegeneración. En estas etapas, aumenta la incidencia de ciertas enfermedades como Alzheimer y Parkinson con deficiencias mentales, ya que se ha demostrado que los estrógenos son primordiales en el mantenimiento de funciones cognitivas, cuyo sustrato neuronal, se ubica en áreas cerebrales como la corteza y el hipocampo (Behl et al., 1997). Se conoce que no hay diferencia alguna entre los niveles de estradiol en aquellas mujeres a las que se les ha provocado la menopausia por tratamiento quirúrgico y aquellas que en forma natural han evolucionado con el paso del tiempo a su etapa de menopausia (Korse et al., 2009).
Esto sugiere que el decremento de las concentraciones de los
esteroides sexuales con el envejecimiento, puede tener un impacto sobre las
funciones del cerebro. De la misma forma se ha propuesto, en animales de
experimentación, que las terapias de sustitución de hormonas gonadales pueden
mejorar la función del cerebro durante el envejecimiento; porque los esteroides
sexuales poseen propiedades que pueden proteger al cerebro de su degeneración
(Green y Simpkins, 2000, Garcia-Segura et al., 2001; Lee y McEwen, 2001).
Estrógenos
en el cerebro
En el cerebro los estrógenos participan en la integridad neuronal y en la
plasticidad del SNC (Brinton, 2001) por sus efectos neurotróficos, la reducción
de la apoliproteína E y beta amiloide, regulación de la acetilcolina, de GABA,
y las aminas biogénicas (noradrenalina, serotonina y dopamina).
Los receptores a estrógenos se localizan en regiones cerebrales como el
hipocampo y la amígdala, reguladores de funciones cognitivas (aprendizaje y
memoria). En la andropausia la disminución de la testosterona reduce la
actividad sexual, la mineralizacion esquelética, la fuerza y masa muscular, un
estado de ánimo deprimido, capacidad de memoria de trabajo y la fluidez verbal.
La somatopausia se relaciona con el descenso en la actividad del eje
somatotrópico, disminución de la masa y fuerza muscular, osteoporosis, aumento de
la grasa corporal, debilidad y fragilidad inmunológica (Lamberts, 2002). A
pesar de estos cambios, un cerebro histológica y bioquímicamente viejo puede
mantener un cierto grado aceptable de funcionalidad.
El envejecimiento neuronal
A medida que se envejece el cerebro y el sistema nervioso periférico,
existe una pérdida natural en la cantidad de neuronas y el peso cerebral. La
transmisión neuronal se hace lenta y a medida que las neuronas van perdiendo su
capacidad de limpieza, se observan cúmulos de lipofuscina3 en los lisosomas y
cierto tipo de proteínas forman filamentos enmarañados (neurofibrilas), así
como agregados amorfos (amiloides), adyacentes a los vasos sanguíneos que
generan alteraciones ligadas a la neurodegeneración. Estos hallazgos se han
encontrado tanto en cerebros de ancianos sanos, como en aquellos con demencias
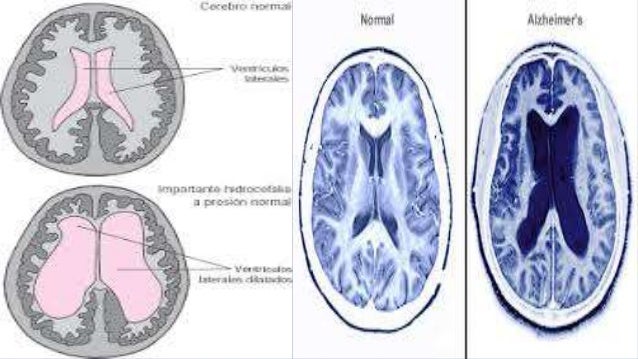
siendo la más común el Alzheimer.
·
Envejecimiento celular en el hipocampo,
como parte del sistema límbico
El hipocampo, es una estructura altamente especializada y susceptible al
envejecimiento y a diferentes estímulos estresantes como la malnutrición
durante su desarrollo.
La malnutrición produce alteraciones anatómicas de las células piramidales
en el hipocampo y en los procesos cognitivos que dependen de éstas. Nuestros
estudios anatómicos muestran que la malnutrición posnatal interfiere con el
proceso celular de las ratas jóvenes, pero se sabe poco acerca de los efectos
de la malnutrición posnatal sobre el aprendizaje de ratas seniles (de 660 días
de edad).
Hemos reportado la interacción que subyace entre la malnutrición posnatal y
la edad sobre el aprendizaje y la
memoria asociad a los cambios subcelulares de las células del CA1 del
hipocampo. Los resultados conductuales muestran que la adquisición
(aprendizaje) y la retención (memoria) están altamente afectadas por la edad.
El análisis morfométrico postmortem de la estructura celular reveló que las
neuronas piramidales del CA1 de los animales malnutridos (jóvenes y seniles)
mostraron áreas significativamente mayores del soma y el núcleo, así como un
número mayor de mitocondrias y lisosomas.
Así, los estudios de envejecimiento celular asociado al daño hipocampal inducido por una dieta baja en proteína administrada por periodo prolongado, mestran la producción de alteraciones subcelulares en las células piramidales del hipocampo que se relaciona con la incapacidad para mantener la memoria a largo plazo en animales jóvenes y seniles malnutridos

Cómo enfrentarse al envejecimiento cerebral:
La principal estrategia es el tratamiento de los factores de riesgo. Cada
día toma más relevancia una adecuada ingesta de antioxidantes, que previenen el
deterioro cognitivo asociado al envejecimiento cerebral. Estos tienen un papel
importante porque atrapan a los radicales libres que son la causa del estrés
oxidativo.
En 1950 el Dr. Denhan Harman, de la Universidad de Nebraska fue el primero
en indicar que los radicales libres son una causa importante del envejecimiento
celular. Su hipótesis, ha recibido amplia confirmación y se ha convertido en
uno de los principales focos de interés en la investigación científica del
envejecimiento y las enfermedades degenerativas.
Los radicales libres se producen de una manera intrínseca en los procesos
normales del organismo: como es el propio metabolismo de los alimentos, la
respiración y el ejercicio y de una manera extrínseca por la contaminación industrial,
el consumo del alcohol y del tabaco, así como de la radiación, de los medicamentos, de los aditivos químicos en
los alimentos procesados de los pesticidas, etcétera.
Por lo que se deben elaborar estrategias preventivas que permitan una mejor
calidad de vida, desde el consumo de alimentos que contengan antioxidantes como
son los que contienen beta carotenos y flavonoides (polifenol), así como las
vitaminas A, B1-B12; C, D y E y los minerales (selenio, zinc, magnesio y
cobre).
Además, los suplementos anti-envejecimiento son alimentos que regulan
transitoriamente los aumentos del cortisol. Por ejemplo, la fosfatidilserina,
es una clase especial de sustancia grasa utilizada por el cuerpo para mantener
la salud de las células nerviosas.
La vitamina A minimiza los niveles de la hormona del estrés. El zinc
participa en la producción de hormonas esteroides como el cortisol. La
L-teanina del té verde mejora la producción de ondas alfa del cerebro.
El Ginseng actúa sobre el cerebro y las glándulas suprarrenales para que
dejen de producir las hormonas del estrés y alimentos ricos en resveratrol del
vino tinto, cacahuates, leguminosas, además de los precursores de
neurotransmisores como la serotonina, triptófano y la colina. Si bien la dieta
juega un papel fundamental para prevenir el envejecimiento cerebral, se requerirá
también de la higiene, el ejercicio, el sueño y evitar el daño oxidativo por el
consumo exagerado del todos los elementos que lo aceleren.
Se sabe, por ejemplo, que en el sueño la etapa de ondas lentas (SOL) va
disminuyendo con la edad. En el varón a los 60 años puede ser mínimo, no así el
sueño de movimientos oculares (MOR) o profundo, el cual se conserva en relación
a la función cerebral. En la mujer se involucran además una serie de cambios
endocrinos dentro de un proceso de estrés oxidativo que incrementa la
producción de radicales libres y la acción de los sistemas antioxidantes
(Liñan, 2004).
Durante el envejecimiento en la mujer se pierden los esteroides sexuales lo
que en parte, puede explicar el deterioro cognitivo y la neurodegeneración en
estas etapas.
Los estrógenos (hormonas esteroideas, por su origen biocinético) actúan
sobre numerosos órganos blanco, como los órganos reproductores, el hueso, el
cartílago, los vasos sanguíneos y el SNC; donde el balance de los
pro/antioxidantes y la desintoxificación de los elementos que ocasionan un daño
potencial pudiera estar regulado por la presencia de estas hormonas (Pajovic y
Saicic, 2008).
Se sabe que los estrógenos como antioxidantes son donadores de hidrógenos
los cuales son utilizados para neutralizar los radicales libres, principalmente
al hidroxilo, por lo que disminuyen los radicales libres y la acción de éstos
sobre las células nerviosas.
Por consiguiente se les puede considerar un soporte para la protección
neuronal, aunque no está bien establecido del todo su mecanismo en situaciones
como la inducción de la muerte celular, el estrés oxidativo, la
excitotoxicidad, la privación de glucosa y la exposición al péptido β-amiloide y
otros agentes neurotóxicos (Woolley., 2007).
Los estrógenos como esteroides neuroactivos que promueven la expresión del
factor de crecimiento nervioso, incrementan el número de conexiones entre las
neuronas, el crecimiento de la propia neurona y funcionan como potentes antioxidantes
gracias a su estructura química semejante al α-tocoferol (Vitamina D) (De
Nicola et al., 2008).
Experimentalmente se ha demostrado que los estrógenos ejercen un efecto
trófico y neuroprotectivo, previniendo del daño neuronal inducido por los
estímulos de los neurotóxicos, así como el inducido por isquemia (Gridley,
Green, Simpkins, 1997; Wang et al., 1999; Kawas et al., 1997), reduce las
lesiones corticales ocasionadas por la exitotoxidad del glutamato (Wang et al.,
1999) o secundario al estado epiléptico, por encefalomielitis autoinmune
(Veliskova et al., 2000, Ito et al., 2001).
Así, los tratamientos con suplementación hormonal son considerados un
importante factor en la protección ante las alteraciones que el envejecimiento
puede llegar a provocar en la mujer.
Comentarios
Publicar un comentario